دانلود مقاله اسیدهای آمینه و متابولیسم آنها بصورت پاورپوینت PPT
عنوان فایل : دانلود مقاله اسیدهای آمینه و متابولیسم آنها بصورت پاورپوینت PPT
نوع فایل : پاورپوینت
حجم فایل : 1.5 مگابایت
تعداد صفحات : 32
مقدمه و معرفی
کلمه اسید آمینه به ترکیبی اطلاق می شود که دارای عامل اسید و عامل آمین باشد. پروتئین ها پلیمر های اسید آمینه های مختلف هستند.
بیست نوع اسید آمینه مختلف وجود دارد که اساس ساختمان همه آنها یکسان است ولی دارای شاخه فرعی یا گروه های متفاوت فرعی هستند.
R- CH(NH2)-COOH در مرکز مولکول اسید آمینه اتم کربن به نام کربن آلفا وجود دارد. این اتم از یک طرف به گروه آمین و از یک طرف دیگر به
گروه کربوکسیل با پیوند کوالان متصل است. سومین پیوند این کربن همیشه با هیدروژن است و چهارمین پیوند به شاخه های فرعی اتصال دارد.
در محلول خنثی گروه کربوکسیل یک پروتون از دست می دهد و گروه آمین یک پروتون به دست می آورد، بنابراین اسیدآمینه در محلول خنثی است
ولی دارای مولکول هایی است که دارای دو بار مختلف الکتریکی هستند و به زویتریون معروف هستند.
برای نامگذاری اسیدهای آمینه تشکیل دهنده پروتئین ها عامل آمین را با لفظ آمینو ذکر کرده و نام اسید را به آن اضافه میکنیم.
مثلاً اسید آلفا آمینوپروپیویک را آلانین می نامند.
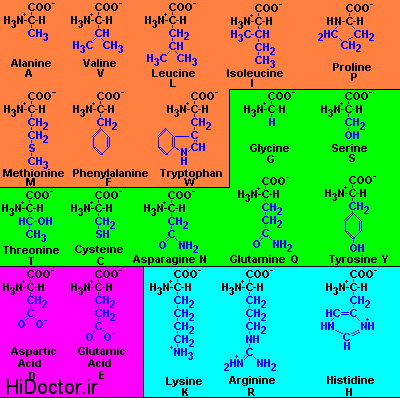
تقسیم بندی اسیدهای آمینه
1-آمینو اسیدهای آلیفاتیک خنثی:
که در ساختمان آنها یک عامل آمین و یک عامل اسید به کار رفته است مهمترین آنها عبارتند از:
گلیسین، آلانین، سرین، ترئونین، والین، لوسین و ایزولوسین.
2- اسید آمینه های گوگرد دار:
قسمت R در ساختمان اسید آمینه گوگرد است . سیستئین و متیونین.
3-اسید آمینه های آروماتیک: فنیل آلانین، تیروزین و تریپتوفان.
4-اسید آمینه های اسیدی:
یک عامل آمین و دو عامل اسید دارند مثل اسید آسپاراتیک و اسید گلوتامیک.
5-اسید آمینه های قلیایی که دارای دو عامل آمین و یک عامل اسید هستند مثل آرژنین، لیزین، هیدروکسی لیزین و هیستدین.
6-ایمینو اسیدها: عامل آمین در ساختمان حلقه شرکت کرده و به صورت NH در آمده مانند پرولین و هیدروکسی پرولین.
در اسیدهای آمینه عامل آمین همیشه به کربن مجاور گروه کربوکسیل وصل است بجز دو اسید آمینه پرولین و هیدروکسی پرولین.
خصوصیات
حلالیت:
تمام اسید های آمینه بجز سیستئین و تیروزین درآب محلول هستند. اسید های آمینه در حلال غیر قطبی نا محلول هستند. تمام اسید های آمینه بجز پرولین و هیدروکسی پرولین در الکل غیر محلول هستند.
نقطه ذوب:
یکی دیگر از خواص فیزیکی اسید های آمینه که به ساختمان آنها بستگی دارد بالا بودن نقطه ذوب آنهاست.
خواص آمفوتر:
هنگامی که اسید های آمینه در آب حل می شود، عامل اسیدی یک پروتون از دست می دهد و عامل آمین یک پروتون به دست می آورد در نتیجه به هر دو به حالت یونیزه در می آیند. اسید های آمینه داراری هر دو گروه کربوکسیل و آمین هستند و بایستی با اسیدها و قلیاها واکنش بدهند. چنین موادی را آمفوتریک می نامند.
پپتید:
اگر دو مولکول اسید آمینه با از دست دادن یک مولکول آب به یکدیگر پیوند یابند ترکیبی پدید می آید که دارای عامل –CO-NH- است، این عامل را اصطلاحاً پیوند پپتیدی می نامند. در این واکنش عامل اسیدی از یک مولکول آمینو اسید با عامل آمین از مولکول دیگر واکنش می دهد. اگر در ساختمان یک مولکول پپتید فقط دو اسیدآمینه باشد آن را دی پپتید، اگر کمتر از 10 تا باشد آن را الیگو پپتید، اگر بیشتر از 10 تاباشد آن را پلی پپتید و بیشتر از 100 تا را پروتئین می نامیم.
برای دانلود مقاله کامل از لینک زیر استفاده نمایید
دانلود مقاله اسیدهای آمینه و متابولیسم آنها 1.5MB


